Por: Randy Alonso Falcón, Oscar Figueredo Reinaldo, Lisandra Fariñas Acosta, Karina Rodríguez Martínez, Sheyla Delgado Guerra Di SilvestrelliEn este artículo: Coronavirus, COVID-19, Cuba, Salud, SARS-CoV-2, Virus
- En video, la Mesa Redonda
- El lunes 19 de abril comienza la aplicación de la tercera dosis de Abdala
- ¿Por qué y para qué Soberana Plus?
- Soberana Plus: Resultados y perspectivas
- Tenemos capacidades para producir suficiente antígeno para hacer los millones de dosis necesarias
- ¿Cómo ocurre el desarrollo de un candidato vacunal?

Para informar sobre los avances del ensayo clínico fase III de Abdala, el ensayo con Soberana Plus en convalecientes y el escalado productivo de los candidatos vacunales cubanos, directivos e investigadores del Centro de Ingeniería Genética y Biotecnología, el Centro de Inmunología Molecular y el Instituto de Hematología comparecen este jueves en la Mesa Redonda.

En video, la Mesa Redonda
El lunes 19 de abril comienza la aplicación de la tercera dosis de Abdala
En una entrevista grabada en Santiago de Cuba para la Mesa Redonda, la Dra. Verena Muzio González, directora de Investigaciones Clínicas del Centro de Ingeniería Genética y Biotecnología (CIGB) dijo que el estudio clínico fase III del candidato vacunal Abdala comenzó el lunes 22 de marzo con la inclusión de los primeros pacientes y la aplicación de la primera dosis entre ese día y el sábado 3 de abril.
En el estudio fueron incluidos 48 291 voluntarios en las provincias de Santiago de Cuba, Granma y Guantánamo, donde se habilitaron 46 vacunatorios en más de 20 unidades asistenciales. “Santiago de Cuba tiene el peso fundamental en el número de voluntarios, con más de 30 000”, precisó.
El lunes 5 de abril comenzó la aplicación de la segunda dosis, que debe culminar este sábado. “Hasta el presente, una de las características que ha tenido el estudio es la buena adherencia de los voluntarios al protocolo de investigación”.
La Dra. Muzio informó que el lunes 19 de abril comienza la aplicación de la tercera dosis de este ensayo. “Como ya se ha dicho en otras ocasiones, tenemos un sistema de vacunación compacto de tres dosis a aplicar cada 14 días, lo que obliga a un ritmo de trabajo con una intensidad superior”.
En los ensayos −dijo la directora de Investigaciones Clínicas del CIGB− participan “una enorme cantidad de especialistas jóvenes, que, si bien no tienen mucha experiencia laboral, sí tienen muchos deseos de aprender y hacer las cosas bien. Considero que es un elemento importante a reconocer. Quiero reconocerlo no solo en los investigadores, sino también en los voluntarios, pues la edades que estamos incluyendo en el estudio, de 19 a 80 años, tenemos también muchos jóvenes que son parte de la investigación como voluntarios, dando también su granito de arena a la investigación.
“Consideramos que el estudio marcha conforme al cronograma previsto y se están ejecutando las acciones según lo establecido. Estamos realmente muy contentos por todo el trabajo que se está haciendo en función de de esta importante investigación”, concluyó sus declaraciones para la Mesa Redonda la Dra. Muzio desde Santiago de Cuba.
¿Por qué y para qué Soberana Plus?
Al comenzar su intervención en la Mesa Redonda, el Dr. Arturo Chang Monteagudo, del Instituto de Hematología e Inmunología (IHI), investigador principal del ensayo clínico Soberana Plus, dijo que desde el principio de la pandemia se recogieron evidencias científicas de que las personas infectados por el Sars-CoV-2, después de padecer la enfermedad COVID-19, podían tener pasado el tiempo una disminución de los anticuerpos protectores y se fue demostrando que era posible la reinfección.
“En nuestro país esto se evidenció tempranamente a través de los estudios del Programa Nacional de Sangre con personas convalecientes donantes de plasma para el tratamiento de otros enfermos, y del Centro nacional de Genética Médica, que había muchos convalecientes con títulos de anticuerpos que ya no eran protectores y, a medida que pasaba el tiempo, iban decayendo los anticuerpos.
“Así es como surge la idea de un candidato vacunal para despertar la inmunidad nuevamente de esas personas que habían estado en contacto por primera vez con el virus. Se diseña Soberana Plus, un candidato vacunal basado en la misma plataforma de Soberana 01 y 02, para despertar los clones de memoria y mejorar la inmunogenicidad en estas personas.
“Hay un segundo valor agregado. Luego se comprueba que no solo es una vacuna útil en convalecientes, sino que puede funcionar como un refuerzo de la inmunidad y ser aplicada, como tercera dosis, a personas que han sido primovacunadas con la Soberana 02 y han recibido dos dosis”.
Soberana Plus: Resultados y perspectivas
Recordó que se comenzó la fase I “para probar de forma primaria la seguridad de este candidato vacunal en 30 personas convalecientes de COVID-19, que tenían bajos niveles inmunitarios. Era un grupo formado por 10 pacientes que habían tenido una COVID-19 ligera, otros 19 una COVid-19 asintomática y 10 que solo tenían anticuerpos IgG contra el virus pero nunca habían tenido un PCR positivo ni un diagnóstico positivo, pero la presencia de esos anticuerpos indicaba que habían estado en contacto con el patógeno”.
En el protocolo se estableció un tiempo de al menos dos meses desde la enfermedad para tener seguridad que los anticuerpos que se detectaban provenía probablemente del efecto de la vacuna y no del efecto de la enfermedad.
“Ese ensayo clínico fase I, que terminó el 13 de febrero y cuyos resultados finales justo se han terminado prácticamente de procesar, se demostró que el candidato vacunal Soberana Plus es muy seguro. Solamente se reportan eventos adversos locales, ningún evento adverso grave relacionado con la vacuna, y se encontró preliminarmente que es un candidato vacunal que en una sola dosis es altamente inmunogénico.
“Las personas que recibieron el candidato vacunal, en su mayoría tuvieron cuatro veces los anticuerpos protectores neutralizantes contra el virus que tenían al principio de la enfermedad; incluso, algunos sujetos elevaron sus anticuerpos hasta 20 veces con respecto a los iniciales.
“Al mismo tiempo, se hicieron ensayos de neutralización viral en los que se encontró que la neutralización de esos anticuerpos contra el virus −claro en un ambiente de laboratorio− podía neutralizar la entrada del virus a la célula”, explicó el especialista.
En la fase II del ensayo clínico, ya aprobada por el Cecmed, se van a incluir 450 convalecientes de COVID-19. “Al mismo tiempo se va a dividir en dos etapas. Una fase II A, en la cual habrá 20 convalecientes entre los 60 y los 80 años de edad, que no habían sido incluidos en el fase I (ninguno de los 30 anteriores tenía más de 60 años). Esta fase II A tiene un diseño muy parecido a un ensayo clínico fase I, porque su diseño está encaminado a demostrar que este candidato vacunal también es seguro en una población de estos grupos de edades.
“Después viene una fase II B, que está condicionada por los resultados de la fase II A. En esta se van a incluir 430 personas y tendrá una característica: sí se va a incluir un placebo. El placebo es una formulación muy parecida a la vacuna, pero que no contiene el antígeno vacunal. Es la única forma de probar en un ensayo clínico que realmente el efecto que se dice que tiene el producto está provocado por el antígeno de la vacuna. Con una particularidad: de estas 430 personas, el placebo solamente serían 86 personas.
“Si los ensayos clínicos no siguieran todas las de la ley, probablemente ya Cuba tendría una vacuna y estuviera vacunada toda su población. Esa es una de la preocupaciones del pueblo: ¿por qué ya no se está vacunando masivamente? No se está vacunando masivamente porque hay que seguir una serie de pasos de investigación para proteger a las personas, y para demostrar que el producto, en este caso la vacuna que se va a licenciar, es un producto seguro, inmunogénico y es eficaz”.
Sobre las perspectivas que ven los especialistas en Soberana Plus, el especialista del IHI afirmó que la principal es proteger a los convalecientes que tienen bajo nivel inmunitario. La segunda es la relacionada con utilizar la Soberana Plus como un refuerzo en personas que han recibido dosis de otras vacunas, “e incluso yo me adelantaría a decir que no solo de la Soberana 02; probablemente, la Soberana Plus sea un buen refuerzo en personas que hayan sido vacunadas con cualquier vacuna.
“Un tercer valor agregado que pudiéramos encontrar en la Soberana Plus, es la producción de la gammaglobulina cubana anti-SARS-CoV-2. Hasta el momento se ha transfundido plasma de personas convalecientes directamente, pero ya se puede producir una gammaglobulina en la cual se purifican los anticuerpos de las personas que han padecido la COVID-19, cuya inmunidad ha sido reforzada con la Soberana Plus, para personas que están en estado grave o crítico en nuestro sistema nacional de salud”.
Tenemos capacidades para producir suficiente antígeno para hacer los millones de dosis necesarias
La Dra. C. Tammy Boggiano Ayo, directora de Desarrollo del Centro de Inmunología Molecular (CIM), señaló que el CIM integró el proyecto de los candidatos vacunales Soberana, sobre todo porque esta institución tiene la capacidad de una biotecnología industrial: todo el proceso en el cual las células son cultivadas a gran escala en condiciones controladas con el objetivo de optimizar su crecimiento y la obtención de la proteína de interés que ellas producen.
“Para lograrlas, a las proteínas que, tanto en el caso de Soberana, como en Abdala y Mambisa, son los antígenos de estas vacunas, es necesario producirlas en células porque son moléculas muy complejas y que no es posible producirlas por síntesis química. Estas moléculas tienen no solo aminoácidos, sino azúcares en su composición, y esa complejidad hace que sea necesario que moléculas como anticuerpos o la misma proteína RBD se produzcan en estas células”, dijo la experta.
Boggiano Ayo explicó que la biotecnología industrial es un proceso que mayormente se realiza en países desarrollados. “La mayoría de las capacidades mundiales, más del 50%, están situadas en Norteamérica y Europa, y luego en Asia. En Cuba se ha venido construyendo todo el desarrollo biofarmacéutico del país en función de tener capacidades que nos permitan producir este tipo de moléculas tan complejas”.
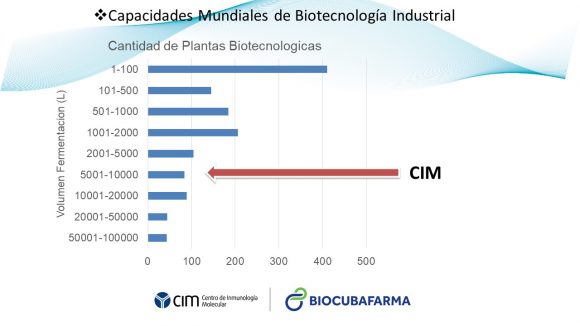
Al respecto, señaló que si se analiza cómo está Cuba en relación a litros de capacidad productiva, puede verse que el país se encuentra entre las pocas plantas que tienen volumen de producción de más de 5 000 litros. “Esto hace que tengamos la posibilidad de producir suficiente antígeno para nuestros candidatos vacunales”.
En el caso de los candidatos vacunales Soberana −dijo−, están involucrados el Instituto Finlay de Vacunas (IFV), que es el promotor de estos preparados, y el CIM, que es el centro que inicia la cadena productiva pues los antígenos se producen en este centro.
¿Cuál es la diferencia entre Soberana 01, Soberana 02 y soberana Plus?
La Dra. Boggiano señaló que tanto en Soberana 01 como en Soberana 02 y Soberana Plus, los antígenos son la RBD.
“En Soberana 01 es un RBD dimérico, la proteína unida a otra igual que ella, por lo que son dos unidades de la misma proteína. Esto hace que las capacidades inmunogénicas sean mayores que si fuera solo una unidad. Es el RBD dimérico más el antígeno de membrana Neisseria Meningitidis tipo B adyuvada en hidróxido de aluminio”, explicó.
En tanto, “Soberana 02 conjuga el RBD monomérico con el toxoide tetánico, también adyuvado en hidróxido de aluminio, mientras que Soberana Plus es la más simple: tiene solo en el RBD dimérico adyuvado en hidróxido de aluminio y es el candidato que se utiliza para tercera dosis o en las personas convalecientes de la enfermedad”.
Según la especialista, tanto el RBD dimérico como el monomérico son producidos por una sola línea celular, donde se introdujo la información genética.
Son células superiores (de mamífero: CHO, células derivadas de ovario de hámster chino) capaces de, luego de serles introducida esta información genética, producir la proteína en un fermentador.
“Ahí es donde controlamos una serie de parámetros como temperatura, pH, oxígeno disuelto. La idea final es que las células estén en un ambiente que se parezca al ambiente en que está en el organismo, y de esta forma ellas puedan multiplicarse y a la vez expresar esa proteína que, originalmente, ellas no tenían en su código genético para expresar, pero que se le introdujo”, dijo.
Refirió que estas células no solo producen el monómero, sino también el dímero y otras muchas proteínas que inicialmente están en este caldo de cultivo. De ahí que un segundo paso sea purificar este caldo de cultivo para obtener solamente la molécula de interés.
“Para hacer todo esto, es necesario empezar por un desarrollo de proceso, que implica diseñar, implementar y reproducir un proceso productivo que entregue consistentemente un producto (proteína) con la capacidad de generar una respuesta inmune y con una calidad específica de pureza, es decir, que no hay ninguna otra proteína o molécula junto a ella al final del proceso.
“Este sistema productivo se diseña primeramente a pequeña escala, en un laboratorio, en un fermentador de mesa de capacidad de dos litros, y se trata de que las células que allí se ponen crezcan lo más que se pueda. En el CIM tenemos un saber hacer previo, que se puede poner en función de la nueva molécula”, explicó.
“Normalmente, todo el desarrollo del proceso puede tardar hasta dos años, incluso más, y el del producto hasta 10 años”, dijo.
Por otra parte, añadió, “el escalado productivo tiene una complejidad industrial y desde el punto de vista ingenieril que es muy importante, y requiere también de un saber hacer para su desarrollo”.
En el caso del CIM, el escalado productivo va de un fermentador de 2 L, a uno de 50 L, a uno de 500 L y finalmente a uno de 2 000 L. “Lograr lo que la gran escala pudiera darle a esa célula, que normalmente es estrés, con el uso del vapor, de velocidades de agitación en el burbujeo, y que en el caso de la gran escala (fermentadores grandes) son mayores que en un fermentador de mesa, es un proceso complejo, pues hay que saber manejar ese estrés de forma tal que la célula realmente reproduzca lo que pasó a pequeña escala: que crezcan y produzcan y luego poder hacer la purificación a esa escala mayor”, explicó.
“Finalmente, luego de purificada, evaluamos la calidad real de la molécula que ya va a pasar a formar parte del proceso de formulación y llenado de la vacuna. Antes de que salga de la institución, tenemos que liberar ese producto con base en las especificaciones de calidad. Este producto se traslada en condiciones de temperatura adecuada y cumpliendo las buenas prácticas de transportación, y luego pasa, en el caso de Soberana 02, al proceso de conjugación, y en el caso de Soberana 01, a la parte de adyuvación, para después formar parte de los candidatos vacunales, procesos en los que intervienen el Instituto Finlay de Vacunas y el Centro de Biopreparados (Biocen)”.
La especialista explicó que el proceso de diseño y producción a pequeña escala comenzó en octubre de 2020 y en diciembre ya estaba concluido. “En estos momentos, estamos en el proceso de escalado hacia los 2000 L, que permitirá obtener toda la capacidad disponible para producir RBD.
“Esta es una actividad multidisciplinaria, tanto para la biología molecular, el desarrollo farmacéutico, la bioquímica, la ingeniería química. Hay que tener experticia en todas estas áreas; de ahí que el equipo de trabajo esté formado por ingenieros, bioquímicos, biólogos y otros especialistas. Tampoco podemos olvidar la importancia del apoyo logístico y los equipos de calidad, pues trabajamos bajo las buenas prácticas de fabricación.
“Tenemos capacidades para producir suficiente antígeno para hacer los millones de dosis necesarias para vacunar a nuestro pueblo, y además podemos tener cierta capacidad extra que pudiéramos utilizar para exportar la vacuna”, concluyó.
¿Cómo ocurre el desarrollo de un candidato vacunal?
Al intervenir en la Mesa Redonda, la Dra. C. Miladys Limonta Fernández, coordinadora de Proyectos de Desarrollo de Candidatos Vacunales en el Centro de Ingeniería Genética y Biotecnología (CIGB), explicó cómo ocurre el desarrollo de un candidato vacunal desde las etapas tempranas.
Tanto los candidatos vacunales Soberana como los del CIGB (Abdala y Mambisa) están basados en la proteína RBD, una parte del virus SARS-CoV-2. Esta estrategia estuvo basada en la plataforma de proteína de subunidad, y en fecha tan temprana como marzo de 2020, ya los biólogos moleculares del CIGB, y desde el diseño de computación, fueron trabajando en posibles proyectos.
“Al inicio teníamos 46 tipos de variantes, teniendo en cuenta las plataformas con que cuenta el CIGB. El centro cuenta con plataformas de expresión de proteínas en bacterias, en levaduras, en células de mamíferos (si bien no a la escala del CIM, en este caso específico), en plantas como biorreactores y en síntesis química.
Todas estas plataformas nos servían como una base para experimentar en cada una de las 46 variantes que estábamos trabajando al mismo tiempo”, dijo.
“En paralelo, teníamos también antecedentes en la historia del CIGB. El centro tiene entre sus plataformas de productos la vacuna contra la hepatitis B; además, la vacuna pentavalente, en la que se combinan cinco antígenos para combatir igual número de enfermedades; la vacuna del Haemophilus influenzae (que se trabajó en conjunto con la Universidad de La Habana y con el laboratorio de síntesis química de la UH, encabezado entonces por el doctor Vicente, hoy director del Instituto Finlay. También se incluyen el Heberbiovac HB y la HeberNasvac, que se utiliza para el tratamiento de la hepatitis B.
“Todos estos productos son parte de la plataforma del CIGB y, por tanto, constituían tecnologías que nosotros podíamos aprovechar para el desarrollo de cada uno de los candidatos vacunales de los que, en un futuro, íbamos a poder disponer para la población cubana”.
Otros de los productos de ese centro científico son el Nasalferón y Jusvinza, que han sido empleados en el combate contra la COVID-19 en Cuba. En el caso de Jusvinza, tiene plataforma en péptidos, mientras que el Herberferón y el Nasalferón tienen plataformas en bacterias.
“El CIGB contaba con una historia muy amplia para abordar toda esta estrategia, teniendo en cuenta la estrategia de desarrollo tecnológico de un producto biofarmacéutico, que se divide en diferentes etapas: la analítica, la escala de banco y en la productiva, donde se producen cantidades diferentes de esos productos. En la escala analítica, son cantidades ínfimas.
“El proceso en esa escala (analítica) puede demorar dos o tres años, porque ahí se realiza el diseño de los experimentos. Es decir, ¿qué condiciones se le van a dar a la célula para que sea capaz de expresar esa proteína que se quiere que se produzca en ese microorganismo? Es ahí que intervienen diferentes variables: la temperatura, el oxígeno disuelto, el pH… En resumen, las condiciones ideales. Eso es lo que se trata de hacer en la escala del diseño experimental de cada una de las variables, donde se obtienen cantidades en microgramos.
Posteriormente transcurre la escala de banco, “donde se establecen las especificaciones. No se puede esperar a etapas tardías (en la escala productiva, por ejemplo) para establecer las especificaciones correspondientes. Debe hacerse en la etapa de banco.
“Pero, ¿qué sucedía? La RBD es una proteína de un virus totalmente nuevo. Entonces, había que trabajar en esta etapa en el establecimiento de las técnicas analíticas. Eso se hizo en paralelo.
“En esa misma etapa de banco es donde obtenemos el producto para hacer los estudios en animales, porque previamente al estudio clínico se requieren determinadas pruebas (toxicidad, seguridad del producto) que se realizan en animales, y en más de una especie. En esta etapa de banco, las cantidades están expresadas en miligramos y se estudia, asimismo, la estabilidad del producto, es decir, del ingrediente farmacéutico activo y después lo que viene a ser el producto.
“Es un proceso que toma tiempo, antes de llegar a la escala productiva, donde se obtiene el producto para el estudio clínico fase III, que es más amplio, y posteriormente se realizan el registro y la comercialización del producto terminado. En esta etapa las cantidades son de gramos. Incluso, hay condiciones productivas con las que se pueden obtener kilogramos de proteínas”.
En el desarrollo de los candidatos vacunales del CIGB, el cultivo se hizo en células de levaduras, con las cuales el centro tiene una gran experiencia de más de 30 años. Gracias a ello en 1991 se obtuvo la vacuna contra la hepatitis B, altamente reconocida a nivel mundial, cuya calidad es reconocida por un competidor, SmithKline, y que hoy es administrada a todos los niños al nacer.
Es un proceso que, además del escalado, incluye técnicas analíticas para medición de pureza, homogeneidad; la fortaleza para medir concentración y las dosis, además de técnicas para medir la seguridad (si el producto es estéril o no, si hay contaminantes como los pirógenos, causantes de fiebre.
“Algo nuevo, que necesitó de la acción coordinada y de la colaboración de varios centros, fue la obtención de materiales biológicos para el desarrollo de los ensayos específicos de los candidatos vacunales. Dependíamos de comprarlos en el exterior o producirlos nosotros mismos. Es la importancia de tener tantos centros científicos y un grupo como BioCubaFarma, esa visión de Fidel de contar con instituciones que pueden colaborar.
“El CIM se dispuso a desarrollar proteínas en células de mamíferos, que se utilizarían en el ensayo para determinar la cantidad de anticuerpos a evaluar ulteriormente por otras técnicas en el estudio clínico. De igual manera, en el CIGB de Sancti Spíritus se desarrollaron anticuerpos para las técnicas a utilizar en la determinación de contaminantes de hospederos. El Centro de Inmunoensayo está jugando igualmente un papel primordial, porque la capacidad de procesamiento que tiene ha permitido evaluar la cantidad de muestras en los estudios clínicos en curso y con una alta eficiencia.
“Igualmente, la colaboración del Centro de Investigaciones de la Defensa Civil permitió que, a partir del aislamiento del virus, se pudiera disponer de una técnica para hacer los estudios de capacidad de neutralización que tienen estos candidatos vacunales ante el reto del virus.
“Todas estas técnicas constituyeron una herramienta que posibilitó efectuar la caracterización físicoquímica del RBD que teníamos al día de hoy. Se va purificando toda la RBD hasta llegar a la pureza que tenemos hoy en el ingrediente farmacéutico activo (IFA) en el candidato vacunal, de más de 99% de pureza medida por diferentes técnicas.
“Después de que se tiene en la escala de banco un IFA en escalas de miligramos, es preciso proceder a los estudios no clínicos. A partir de que se van obteniendo las primeras cantidades, se empiezan a hacer los estudios de farmacología, de manera tal que permitan probar el concepto de la proteína que se está obteniendo. Es decir: ¿realmente levanta anticuerpos? Esa es una pregunta que debemos hacernos con este tipo de antígenos.
“Es una vacuna y las vacunas están diseñadas para levantar anticuerpos. Es importante medir entonces, en etapas tan tempranas, en especies de animales, este concepto.
“Igualmente es importante medir la toxicidad. ¿Cómo la medimos: con una dosis única, con dosis repetidas…? Es, precisamente, a partir de un diseño de dosis, hasta cien veces de las que vamos a usar en humanos, poderlas aplicar a un animal y ver el resultado. Eso se va haciendo desde esta etapa más temprana. Estudios de toxicidad a dosis repetidas, en primates no humanos, así como estudios de tolerancia local y de toxicidad de la reproducción en ratas. Son estudios no clínicos que se hacen a la par, previamente a la presentación del expediente”, explicó.
“Una vez que teníamos la proteína, hicimos la solicitud de aprobación de inicio de estudios clínicos ante la autoridad reguladora. En octubre del 2020,transferimos la producción de la escala de banco a la escala productiva en la planta del CIGB. Completada la escala productiva, se comienza, a partir de la aprobación de la autoridad reguladora, los estudios clínicos de Abdala”.
Sobre la evolución clínica de este candidato vacunal, señaló que el 7 de diciembre comenzaron los ensayos clínicos de Abdala y Mambisa. Las fases I y II de Abdala transcurrieron entre diciembre y marzo. El 1ro. de mayo, en el fase III, debe administrarse la tercera dosis, tras comenzar su aplicación el 19 de abril.
“Marzo de 2021 −recordó− marcó el inicio del escalado final del IFA de Abdala, en el fermentador de 3 000 litros”.
La directiva destacó también el candidato vacunal Mambisa, el cual incluye también en su composición como ingrediente farmacéutico activo el RBD, y que es uno de los cinco candidatos vacunales en el mundo que utilizan la vía nasal. “Terminamos el ensayo clínico fase I en el que se demostró en 88 individuos su seguridad y tolerancia”.
Actualmente, transcurre el proceso para presentar ante la autoridad reguladora un estudio, fases I-II, para emplear ese candidato vacunal como dosis de refuerzo en convalecientes. La vía de administración es nasal.
“Otra aplicación de Mambisa puede ser como dosis de refuerzo en la combinación de otras vacunas. Por ejemplo, Sputnik V, la vacuna rusa, pudiera combinarse con Mambisa, y quizás en un futuro transnacionales como Pfizer y Moderna podrían interesarse.
“Cuba es el único país del mundo que se ha ocupado de los convalecientes y de este tipo de aplicación”, subrayó.
Estudios han demostrado cómo las dosis de refuerzo elevan los niveles de anticuerpos en las personas. “Esto va en sintonía con lo que estamos aplicando, al utilizar dosis de refuerzo en esquemas de vacunación desde el principio”.
Por último, informó que el CIGB está trabajando en relación con las variantes. “Es decir, a esta misma proteína se le incluye la información genética de los mutantes (B1-7 y B1-351). A partir de abril se va a trabajar en el escalado de ese posible candidato que incluye los mutantes, porque la plataforma tecnológica nos permite avanzar en esta dirección con las tecnologías que dominamos”.
fuente: http://www.cubadebate.cu/noticias/2021/04/15/como-marchan-los-ensayos-clinicos-y-el-escalado-productivo-de-los-antigenos-de-los-candidatos-vacunales-cubanos-video/#anexo-1530191
GRACIAS Paquita Armas Fonseca



